Se llaman compuestos meso a aquellos que tiene átomos de carbónos asimétricos pero son aquirales. En estos casos, la imagen especular de estos, es en si, el mismo compuesto. Este tipo de compuestos no presenta actividad óptica y presentan un plano de simetría que divide en dos la molécula. Los compuestos meso se basan en en el número de centros estereogénicos representado por la fórmula de 2 a la n, n siendo el número de centros quirales para determinar la cantidad de estereoisómeros que tiene la molécula. Uno de los requisitos de los compuestos meso es tener por lo menos dos sustituyentes en común. Aunque este es un requisito, hay compuestos que presentan esta característica y no son compuestos meso.
Por ejemplo, en el 2,4-pentanodiol, tanto el segundo y cuarto átomos de carbono, que tienen estereocentros, tienen los cuatros sustituyentes en común.
Dado que un isómero meso tiene una imagen especular superponible, un compuesto con un total de n estereocentros no puede tener 2n estereoisómeros, dado que uno de ellos es meso.
miércoles, 20 de mayo de 2009
Proyecciones Fischer
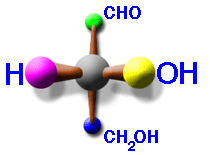
Mediante la proyeccion, una molécula es dibujada en un plano a dos dimenciones. Cuando la molecula es dibujada en forma de cruz, es una proyeccion de FIscher, ya que las moleculas se encuentran en línea recta. Los sustituyentes van entonces al fondo del plano en la línea vertical. En la línea horizontal se colocan los grupos que salen hacia nosotros, quedando en medio el carbono proyectado.
En la química organica, las proyecciones de Fischer se usan para representar un carbono unido a cuatro sustituyentes distintos. Estos átomos constituyen centros quirales. En una proyección de Fisher se representa cada carbono quiral con sus cuatro sustituyentes dispuestos en cruz aplicando la siguiente convención:
- Los sustituyentes situados a derecha e izquierda sobresalen del plano de representación (papel o pantalla) y en el espacio estarían situados por delante de dicho plano, hacia el observador.
- Los sustituyentes representados arriba y debajo del centro quiral estarían situados espacialmente detrás del átomo quiral.

Proyecciones de Haworth

Reciben el nombre de proyecciones de Haworth las moléculas que giran alrededor de monosacáridos pequeños en forma lineal ( proyecciones de Fischer). En lo que llamamos representación de Haworth, se puede observar la cadena carbonada situada sobre un plano, situandose los radicales a un lado o por encima.
Esta estructura ciclada se puede obtener de hexosas y aldopentosas. El enlace de ciclación se genera entre el carbono que posee el grupo funcional y el carbono asimétrico más alejado del grupo funcional.
La proyección Haworth es comunmente usada para representar hemiacetales. Esta esta presente en los glúcidos también.
Nomenclatura R-S(1)
La nomenclatura R-S (1) determina la configuración absoluta de los carbonos quirales. Esta fue creada por los químicos Cahn, Ingold y Prelog.
Para nombrar los compuestos se deja el grupo de prioridad menor (d) hacia atrás y se observa el sentido de giro para ir desde el grupo de más prioridad (a) hacia el de menor (c) de los tres que quedan. Si el sentido es el de las agujas del reloj, la configuración es R (rectus). Al contrario es S (sinister).El número atómico de los átomos directamente unidos al estereocentro determina su orden de prioridad. El átomo de mayor numero atómico tiene la mayor prioridad. Si uno de ellos es un hidrógeno, éste será el de prioridad menor.Si hay dos átomos iguales unidos al estereocentro, se observa en la posición siguiente qué atomo tiene el número atómico mayor. En caso de nueva coincidencia se sigue a la siguiente posición, y así sucesivamente. Si alguno de los átomos unidos al estereocentro participa en un enlace doble o triple, se supone que aquél está unido por enlaces sencillos a un numero respectivamente doble o triple de átomos.Para determinar la configuración R/S nos situamos frente a la molécula. Numeramos por el orden de prelación habitual los sustituyentes de la parte delantera y trasera independientemente. Primero los de delante (1 y 2) y luego los de detrás (3 y 4). El sentido de giro para ir de 1 á 2 y 3 nos da la configuración.
 Por: Marcela Muñoz
Por: Marcela Muñoz
Para nombrar los compuestos se deja el grupo de prioridad menor (d) hacia atrás y se observa el sentido de giro para ir desde el grupo de más prioridad (a) hacia el de menor (c) de los tres que quedan. Si el sentido es el de las agujas del reloj, la configuración es R (rectus). Al contrario es S (sinister).El número atómico de los átomos directamente unidos al estereocentro determina su orden de prioridad. El átomo de mayor numero atómico tiene la mayor prioridad. Si uno de ellos es un hidrógeno, éste será el de prioridad menor.Si hay dos átomos iguales unidos al estereocentro, se observa en la posición siguiente qué atomo tiene el número atómico mayor. En caso de nueva coincidencia se sigue a la siguiente posición, y así sucesivamente. Si alguno de los átomos unidos al estereocentro participa en un enlace doble o triple, se supone que aquél está unido por enlaces sencillos a un numero respectivamente doble o triple de átomos.Para determinar la configuración R/S nos situamos frente a la molécula. Numeramos por el orden de prelación habitual los sustituyentes de la parte delantera y trasera independientemente. Primero los de delante (1 y 2) y luego los de detrás (3 y 4). El sentido de giro para ir de 1 á 2 y 3 nos da la configuración.
 Por: Marcela Muñoz
Por: Marcela Muñoz
Nomenclatura DL
La nomenclatura DL sirve para designar la configuración electrónica de un isómero con solo un carbono asímétrico. Por medio de este tipo de nomenclatura, al isomero que tiene el grupo funcional a la derecha se le llama D. De este mismo modo, al isómero con el grupo funcional a la izquierda, se le llama L. Aunque puede llegar a coincidir, este tipo de nomenclatura no indica si el compuesto es dexógiro o levógiro. Por ejemplo, en el caso del gliceraldehído, el isomero D resulta ser dexógiro y se representa con el signo (+) , pero aunque existen estos casos, no siempre es asi.
Cuando el isomero tiene más de un carbono asimetrico, es mejor usar otro tipo de nomenclatura, como el sistema propuesto por Cahn, Ingold y Prelog.
miércoles, 13 de mayo de 2009
El Polarizador

Como su nombre lo indica, la función de un polarizador es polarizar la luz que pasa a traves de el. Funciona como un filtro, eliminando todas las direcciones de vibración de la luz menos una. Con esto se eliminan los reflejos y se da mas potencia al haz de luz resultante ya que toda la luz antes dispersa esta concentrada en un rayo.
Este consta de un lente que se hace girar, determinando la dirección de la luz. Usando dos lentes, es posible bloquear la luz si estos se colocan de manera paralela y girando uno conreferencia la angulo del otro, ya que varia el plano de polarización.
Los polarizadores se usan con frecuencia en camaras fotograficas, laser, lentes 3D, microscopios, etc.
Al crear este efecto sobre la luz, se puede lograr intensificar los colores, sobretodo si hablamos de lentes fotograficas.
Sustancias levógiras y dextrógiras.
Las sustancias que presentan actividad optica son aquellas que cuando un plano de loz polarizada las atraviesa, generan un plano de vibración de la luz. Estas sustancias pueden ser levógiras o dextrógiras. La diferencia entre estas dos se encuentra en la direccion hacia la que giran el plano de polarización. Las dextrógiras hacen girar el plano hacia la derecha mientras que las levógiras lo giran hacia la izquierda.
La causa de este efecto optico es la asimetria molecular de las sustancias. La presencia de un carbono asimetrico es lo que causa esta asimetria en la quimica organica.
Esto puede ser observado en los espejos, los cuales hacen que, al filtrarse la luz, gire hacia la derecha o hacia la izquierda. Esto hace que la luz se polarize y gire, perdiendo asi los vectores.
La causa de este efecto optico es la asimetria molecular de las sustancias. La presencia de un carbono asimetrico es lo que causa esta asimetria en la quimica organica.
Esto puede ser observado en los espejos, los cuales hacen que, al filtrarse la luz, gire hacia la derecha o hacia la izquierda. Esto hace que la luz se polarize y gire, perdiendo asi los vectores.
martes, 12 de mayo de 2009
Determinación de concentraciones con polarímetro
Un polarimetro se usa para determinar el valor de de la desviacion de luz polarizada por un enantiomero. Los polarimetros se usan para determinar rapida y precisamente la concentracion de una sustancia en una solucion opticamente activa.
Un polarímetro sencillo consta de una fuente de luz, un polarizador, un analizador y las lentes y diafragmas necesarios para regular el haz de luz. La sustancia que se quiere estudiar se coloca entre el polarizador y el analizador, y si se trata de un líquido se introduce en un tubo de longitud conocida.
Este se utiliza en medicina, quimica e industrias como la azucarera.
Un polarímetro sencillo consta de una fuente de luz, un polarizador, un analizador y las lentes y diafragmas necesarios para regular el haz de luz. La sustancia que se quiere estudiar se coloca entre el polarizador y el analizador, y si se trata de un líquido se introduce en un tubo de longitud conocida.
Este se utiliza en medicina, quimica e industrias como la azucarera.
Luz Polarizada

Definicion:
Para definir que es la luz polarizada, es importante explicar el fenomeno de polarización. La polarizacion electromagnetica puede ocurrir en ondas electromagneticas, oscilando en un plano determinado llamado plano de polarizacion. Siendo la luz energia electromagnetica radiante, la polarizacion se puede producir en sus ondas, dando coo resultado luz polarizada.
La luz polarizada consiste en fotones individuales cuyos vectores de campo electrico se encuantran alineados y en la misma direccion. En la luz laser, los fotones se emiten coherentemente, por lo tanto esta es polarizada. Cuando los fotones son emitidos aleatoriamente la luz es normal.
La polarizacion puede verse en cristales determinados que son transparentes de forma individual pero si se colocan alineados paralelamente, cada uno girado con un angulo referente al otro la luz no puede atravesarlos, siendo 90º el angulo de obscuridad total.
La polarizacion tambien se da con la reflexion de luz.
El ojo humano es incapaz de distinguir entre luz normal y luz polarizada.
viernes, 24 de abril de 2009
mezcla racemica y sintesis enantioselectiva- calculo de estereoisomeros
Una mezcla racémica es una mezcla que contiene cantidades iguales de dos enantiómeros y es a simple vista inactiva. Una mezcla racémica es una mezcla en la cual productos de una reacciòn quìmica con un poco de actividad òbtica debido a isomerismo, es decir que estan precentes en un 50%.Un enantiómero con un centro quiral, y un poco de actividad puede hacer girar la luz polarizada creo que por el efecto de vipolaridad, pero tamvien por lo de los isomeros.Aunque en realidad no todos los estereoisómeros hacen que la luz se desvie aunque la mayoria de estos si lo hacen.Luis Pasteur fue el primero en descubrir esta propiedad en 1847 cuando sólo contaba con 25 años de edad. Siendo la primer mezcla racémica la del àcido racèmico.
CONCEPTOS IMPORTANTES PARA ENTENDER:Isomería: La isomería es una propiedad de algunos compuestos quìmicos que con la misma formula quimica , iguales que los àtomos , presentan estructuras moleculares distintas. Estos compuestos forman los que reciben el nombre de isòmeros.Quiralidad:La quiralidad es cuando no se puede sobre poner en el mismo porque segun yo por el reflejo de espejo.
Por:Roberto Huerta
___________________-
Para calcular el numero de estereoisomeros en un compuesto es necesario saber cuantos carbonos asimetricos contiene,ya que la relacion es proporcional. Por ejemplo, cuando hay 2 carbonos asimetricos el numero de estereoisomeros es 4 y si se tienen 3 carbonos asimetricos el numero de estereoisomeros es 8. Tomando eso como referencia podemos concluir que la formula para sacar el numero total de estereoisomeros en un compuesto es 2 elevado al numero de carbonos asimetricos que contenga el compuesto.
por: marcela Muñoz
CONCEPTOS IMPORTANTES PARA ENTENDER:Isomería: La isomería es una propiedad de algunos compuestos quìmicos que con la misma formula quimica , iguales que los àtomos , presentan estructuras moleculares distintas. Estos compuestos forman los que reciben el nombre de isòmeros.Quiralidad:La quiralidad es cuando no se puede sobre poner en el mismo porque segun yo por el reflejo de espejo.
Por:Roberto Huerta
___________________-
Para calcular el numero de estereoisomeros en un compuesto es necesario saber cuantos carbonos asimetricos contiene,ya que la relacion es proporcional. Por ejemplo, cuando hay 2 carbonos asimetricos el numero de estereoisomeros es 4 y si se tienen 3 carbonos asimetricos el numero de estereoisomeros es 8. Tomando eso como referencia podemos concluir que la formula para sacar el numero total de estereoisomeros en un compuesto es 2 elevado al numero de carbonos asimetricos que contenga el compuesto.
por: marcela Muñoz
Centros quirales y Carbonos asimetricos
Cuando una molecula tiene un centro quiral cuando el atomo esta unido a cuatro sustituyentes diferentes. Las moleculas con centro quiral tienen una imagen especular o inversa llamada enantiomero y no se puede superponer. Los centros quirales tambien reciben el nombre de carbonos asimetricos. Cuando un compuesto tiene centro quiral se pueden formar por lo menos dos tipos de estereoisomeros. Una molecula puede tener varios estereocentros y estar formado por enantiomeros, isomeros opticos y diasteroisomeros.
Los compuestos que teniendo carbonos asimetricos tambien son aquirales, presentando un plano de simetria, se llaman compuestos meso.
Cuando solo hay un carbono asimetrico solo puede haber un par de formas quirales o enantiomeros, por lo tanto si una molecula tiene n numero de atomos de carbono asimetricos el numero de isomeros opticos es 2n (2 a la n).
Los compuestos que teniendo carbonos asimetricos tambien son aquirales, presentando un plano de simetria, se llaman compuestos meso.
Cuando solo hay un carbono asimetrico solo puede haber un par de formas quirales o enantiomeros, por lo tanto si una molecula tiene n numero de atomos de carbono asimetricos el numero de isomeros opticos es 2n (2 a la n).
jueves, 23 de abril de 2009
Estereoisomeros y Diasteroisomeros
Un estereoisomero es un isomero de una molecula con las mismas conexiones entre atomos pero diferente orientacion en el espacio.
Se conoce como estereoisomeria a la isomeria en el espacio, ya que con estos isomeros, es necesario representarlos en el espacio para que las diferencias estructuralesse puedan apreciar. Se clasifica en configuracional y conformacional. Del mismo modo, la isomeria configuracional se divide entre estereoisomeria optica y estereoisomeria geometrica.
Los diastero isomeros son estereoisomeros de la rama de los isomeros configuracionales. No se pueden superponer ni presentan una imagen especular y por lo tanto son diferentes de los enantiomeros. Una sola molecula puede tener varios estereocentros. Las aldohexosas, los carbohidratos y los azucares de seis carbonos son ejemplos de diasteroisomeros.
Se conoce como estereoisomeria a la isomeria en el espacio, ya que con estos isomeros, es necesario representarlos en el espacio para que las diferencias estructuralesse puedan apreciar. Se clasifica en configuracional y conformacional. Del mismo modo, la isomeria configuracional se divide entre estereoisomeria optica y estereoisomeria geometrica.
Los diastero isomeros son estereoisomeros de la rama de los isomeros configuracionales. No se pueden superponer ni presentan una imagen especular y por lo tanto son diferentes de los enantiomeros. Una sola molecula puede tener varios estereocentros. Las aldohexosas, los carbohidratos y los azucares de seis carbonos son ejemplos de diasteroisomeros.
Isomeria- Enantiometro
La isomeria es la propuedad que poseen algunos compuestos que tienen la misma formula quimica o molecular pero con dferentes propiedades o estructura. Estos compuestos se llaman isomeros. Por ejemplo: alcohol etilico y el eter dimetilico. Algunas ramas que se derivan de la isomeria son: Isomeros constitucionales; son los mismos atomos pero con distintaconectividad.Estereoisómeros; los mismos atomos tambien pero con diferente posicion espacial.Isomería conformacional; estos tienen diferentes conformaciones.Isomería configuracional; estas son diferentes configuraciones.Enantiómeros; son estereoisómeros que son especulares, una es comoel reflejo de la otra en un espejo.Diastereoisómeros; estas son estereoisómeros tambien pero no sonimagenes especulares.
Por: Marcela Muñoz
Los enantiomeros normalmente se caracterizan por poseer un átomo unido a cuatro grupos distintos llamado asimétrico o quiral. Algunos ejemplos de estos son: la presencia de un carbono asimétrico, hace posible que la molécula y su imagen especular sean distintas. En realidad eso significa que la contraparte de la molecula se ve como si esta se reflejara en un espejo. Los anantiòmeros son como un espejo en una isomeria, haciendo que la molécula y su imagen especular sean distintas. Los enantiómeros se suelen representarse por medio de la proyección de Fisher. Un enantiómero que rota el plano de la luz polarizada hacia la derecha se dice que es dextrorrotatorio o dextrógiro, y suele colocársele al nombre de éste una letra de minúscula o un signo positivo. Si lo hace hacia la izquierda, es levorrotatorio o levógiro y suele colocársele al nombre una letra ele minúscula (l), o un signo negativo (-). Depende de la direccion del reflejo el nombre y la nomenclatura que se le da.
Por: Roberto Huerta
Por: Marcela Muñoz
Los enantiomeros normalmente se caracterizan por poseer un átomo unido a cuatro grupos distintos llamado asimétrico o quiral. Algunos ejemplos de estos son: la presencia de un carbono asimétrico, hace posible que la molécula y su imagen especular sean distintas. En realidad eso significa que la contraparte de la molecula se ve como si esta se reflejara en un espejo. Los anantiòmeros son como un espejo en una isomeria, haciendo que la molécula y su imagen especular sean distintas. Los enantiómeros se suelen representarse por medio de la proyección de Fisher. Un enantiómero que rota el plano de la luz polarizada hacia la derecha se dice que es dextrorrotatorio o dextrógiro, y suele colocársele al nombre de éste una letra de minúscula o un signo positivo. Si lo hace hacia la izquierda, es levorrotatorio o levógiro y suele colocársele al nombre una letra ele minúscula (l), o un signo negativo (-). Depende de la direccion del reflejo el nombre y la nomenclatura que se le da.
Por: Roberto Huerta
Isomeros Opticos

La esteroisomeria optica se presenta cuando en un compuesto hay por lo menos un atomo de carbono asimetrico. Los isomeros opticos no pueden ser superpuestos ya que uno es la imagen especular del otro, por lo que recibe el nombre de molecula quiral. Estas moleculas pueden ser diferenciadas solamente por su efecto sobre la luz, ya que tienen las mismas propiedades fisicas y quimicas. Al girar en direccion contraria, desvian el plano de la luz polarizada en diferente direccion. Uno gira hacia la derecha y es representado con la letra R; el otro gira hacia la izquierda y se representa con la letra S. Este tipo de nomenclatura es llamado Nomenclatura R, S y sirve para determinar la configuracion absoluta de los carbonos quirales.
Las moleculas que presentan simetria son conocidas como aquirales y son opticamente inactivas.
Las moleculas con un estereocentro siempre son quirales.
Las moleculas que presentan simetria son conocidas como aquirales y son opticamente inactivas.
Las moleculas con un estereocentro siempre son quirales.
Suscribirse a:
Comentarios (Atom)